|
Avertissement
|
|||
|
Si vous arrivez
directement sur cette page, sachez que ce travail est un rapport
d'étudiants et doit être pris comme tel. Il peut donc
comporter des imperfections ou des imprécisions que le lecteur
doit admettre et donc supporter. Il a été
réalisé pendant la période de formation et
constitue avant-tout un travail de compilation bibliographique,
d'initiation et d'analyse sur des thématiques associées
aux technologies biomédicales. Nous
ne
faisons
aucun
usage
commercial
et
la
duplication
est
libre.
Si
vous
avez
des
raisons
de
contester
ce
droit
d'usage, merci
de nous en faire part . L'objectif de la
présentation sur le Web est de
permettre l'accès à l'information et d'augmenter ainsi
les échanges professionnels. En cas d'usage du document,
n'oubliez pas de le citer comme source bibliographique. Bonne
lecture...
|
|||
|
|
|||
|
|||
|
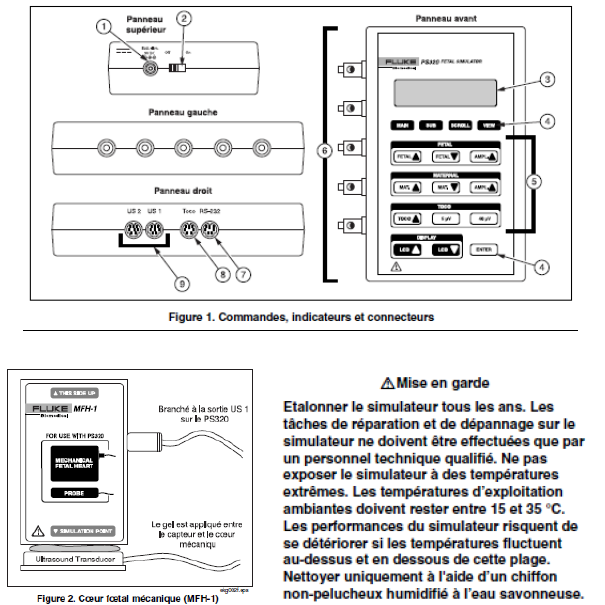
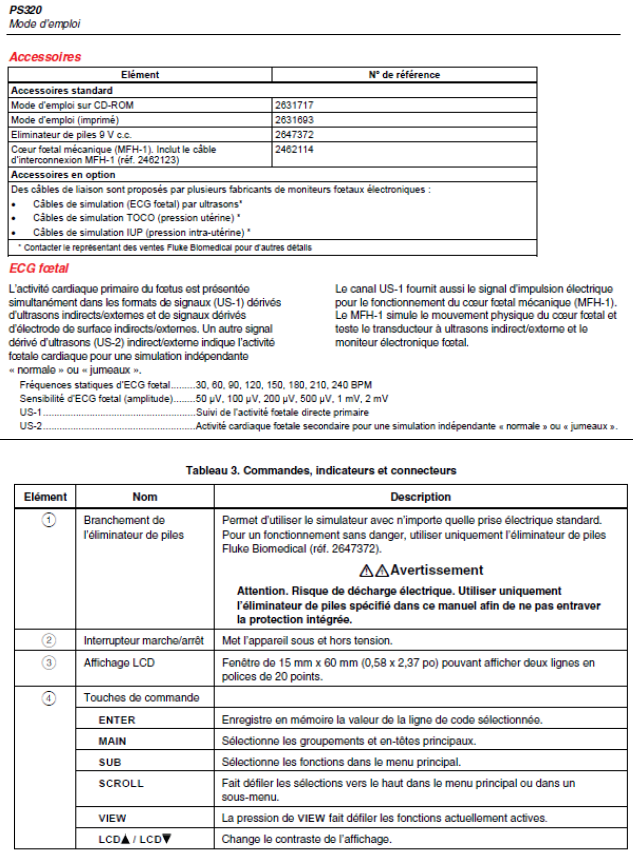
Référence
à rappeler : Détermination de la criticité des D.M
et C.Q sur cardiotocographe, VILA Christophe
Stage, Certification Professionnelle ABIH, UTC, 2011 URL : http://www.utc.fr/abih ; Université de Technologie de Compiègne |
|||
|
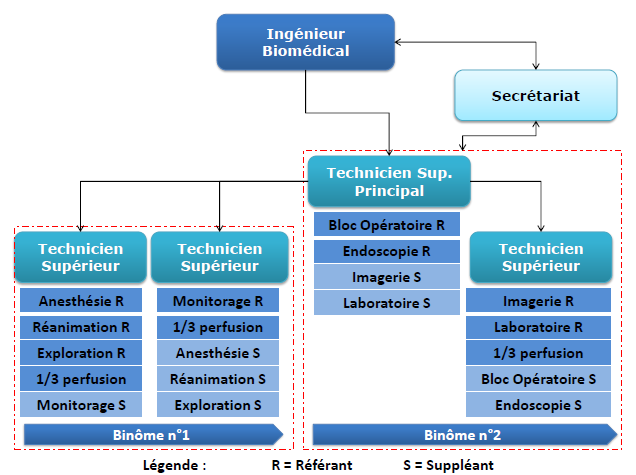
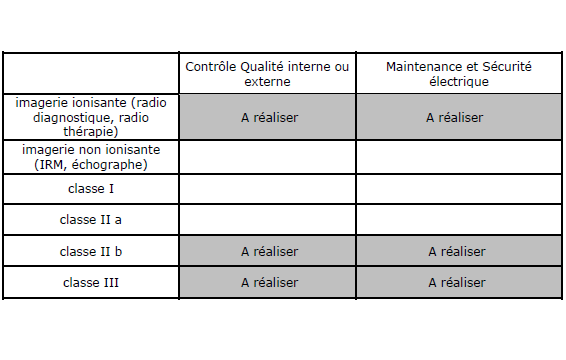
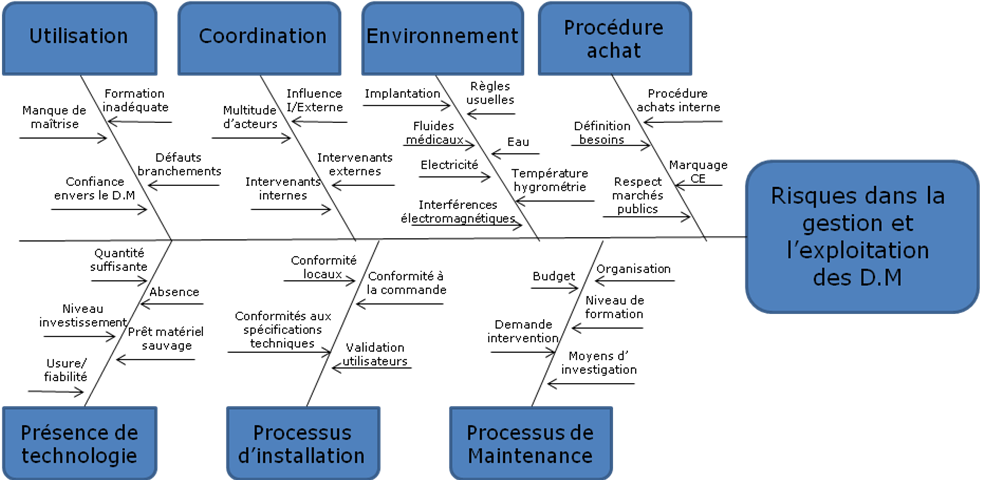
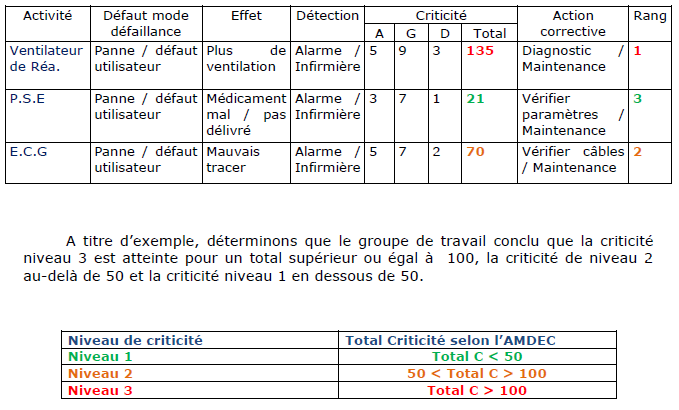
Après avoir pris
connaissance des risques
liés à l’utilisation et à la gestion des
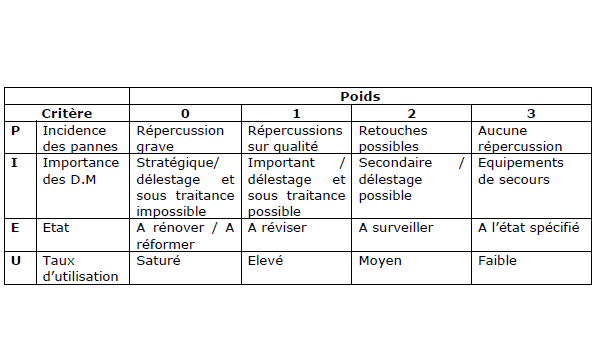
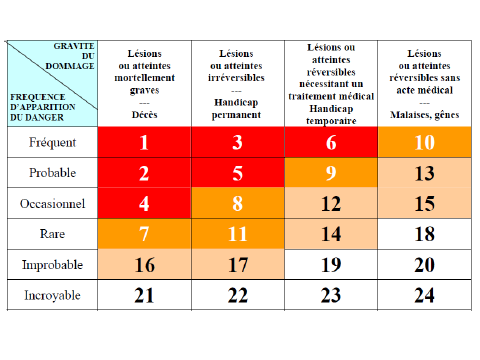
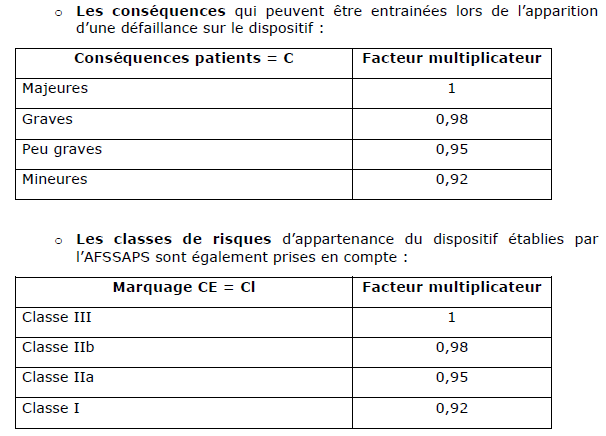
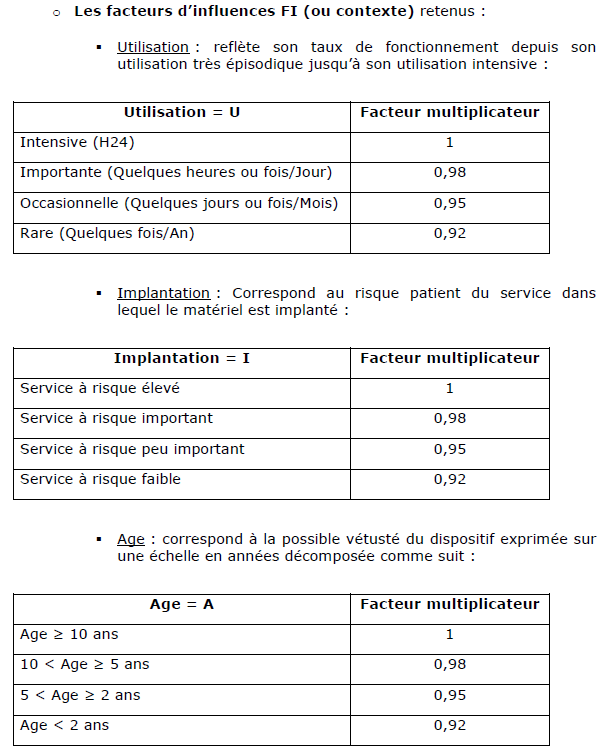
dispositifs médicaux, j’ai pu réaliser une méthode
permettant de déterminer la criticité des
équipements.
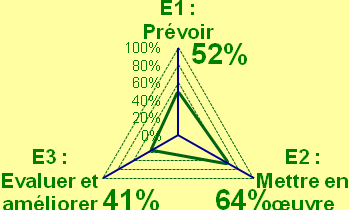
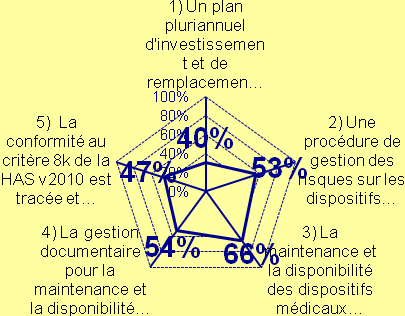
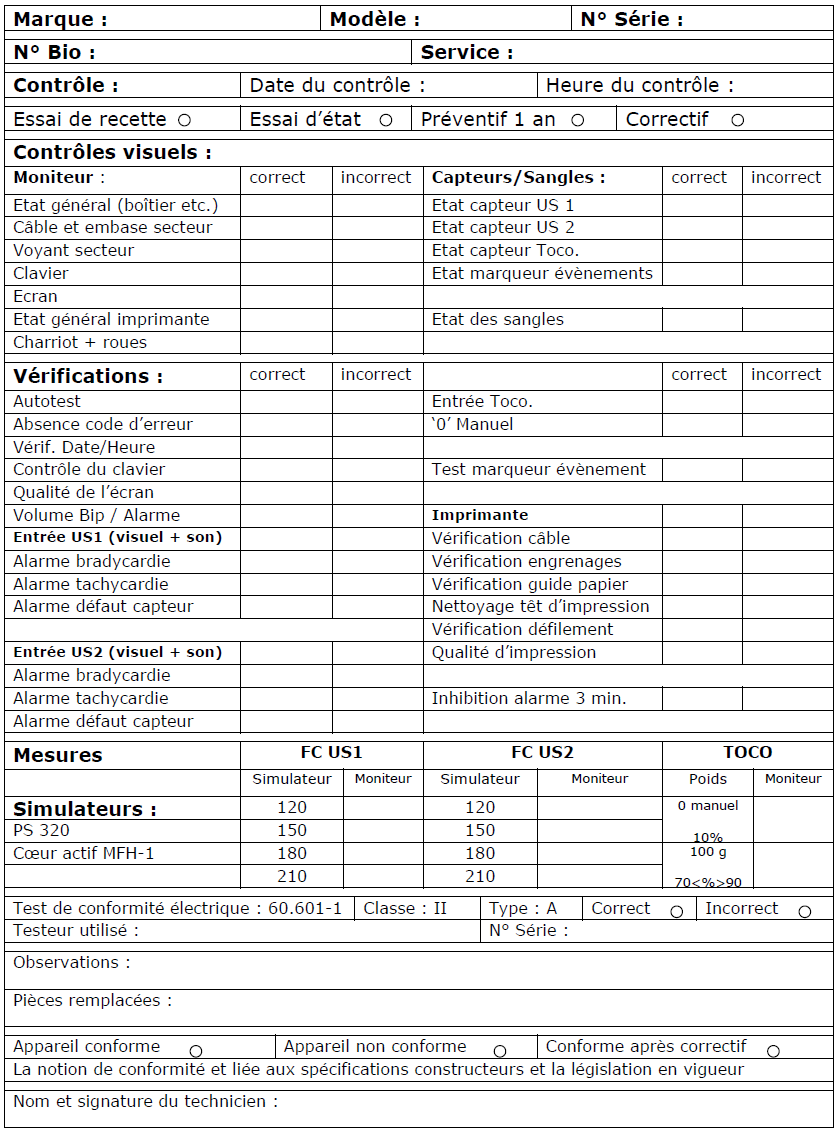
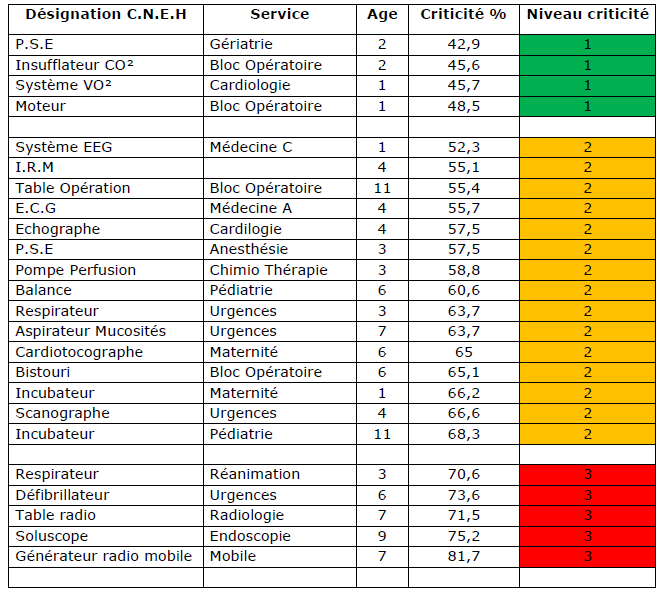
Suite à l’autodiagnostic concernant le critère 8K de l’HAS sur le service biomédical, j’ai pu proposer des axes d’améliorations. Enfin, mon rapport se termine par l’élaboration d’un contrôle qualité sur les cardiotocographes. Mots Clés :
Criticité, Dispositif médical, 8K, Contrôle
Qualité, Cardiotocographe
|
|||
|
After noting the risks
associated with the use and
management of medical devices, I have achieved a method for determining
the criticality of the equipment.
Following the diagnostic criteria for the 8K of HAS on bio-medical service, I was able to propose axes of improvements. Finally, my report ends by the elaboration of quality control on cardiotocographs. |